使用注意事项:
1. 本试剂盒请在0-5 ℃储存。
2. Biotin-(AC5)2Sulfo-OSu溶液需要现配现用 (由于Biotin-(AC5)2Sulfo-OSu易水解,尽量避免在水溶液的状态保存)。
3. 标记好的蛋白质请在0-5 ℃保存 (加入0.1%的叠氮钠等防腐剂)。
使用步骤:
1. 配制溶液
1) NaHCO3缓冲液
在含有NaHCO3粉末的容器中加入10ml超纯水溶解。
2) PBS缓冲液
在100ml容量瓶中加入1片PBS,先用少量超纯水溶解后,再用超纯水补充至100ml,制成10mmol/l的PBS缓冲液。
3) 蛋白质溶液
在样品管中精确称量1.0-5.0mg蛋白质并记录称量值后,用移液器加入500μl操作步骤1)中的NaHCO3缓冲液。盖上盖子后,用漩涡振荡器等搅拌溶解蛋白质。
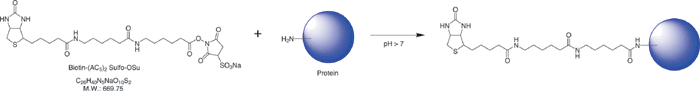
4) Biotin-(AC5)2Sulfo-OSu溶液
在1支含有Biotin-(AC5)2Sulfo-OSu的管子中加入适量纯水溶解。为了控制标记率,根据不同的标记对象,请参考表1调整Biotin-(AC5)2Sulfo-OSu溶液的浓度及加入量。
*由于Biotin-(AC5)2Sulfo-OSu易水解,溶解后请尽快标记。
2. 生物素标记操作方法
1) 请参考表1在配制好的蛋白质溶液中加入合适浓度和用量的Biotin-(AC5)2Sulfo-OSu溶液。
2) 盖紧盖子充分混合后,在25 ℃水浴恒温摇床中培养2h。
表1 Biotin-(AC5)2Sulfo-OSu标记各种蛋白质的标记率
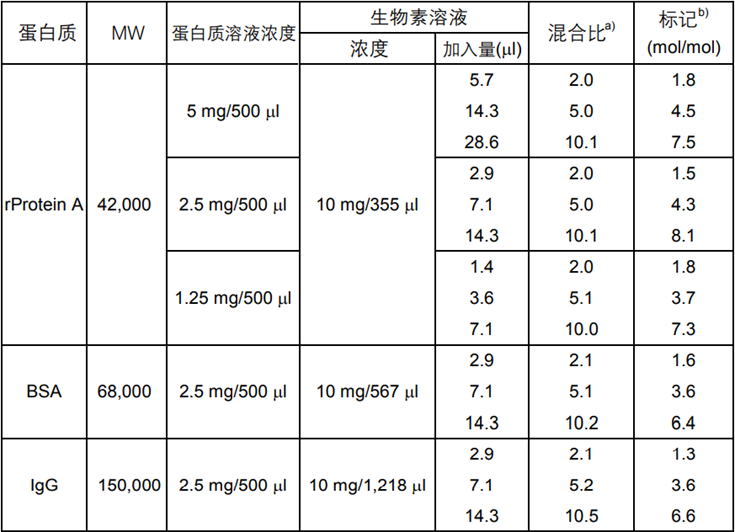
以上数据为本公司实际检测的结果,如实验条件变动,
结果有可能改变。标记率是根据HABA法测得。
a) 1mol蛋白质:生物素的摩尔数
b) 1mol蛋白质上所结合的生物素的摩尔数
3. 蛋白质标记后的凝胶过滤纯化
1) 打开层析柱上的盖子,弃去填充液。
2) 打开层析柱出口的盖子,用PBS分数次洗脱,每根层析柱收集大约10ml的洗脱液,使凝胶平衡。
3) 用移液器吸取500μl标记好的蛋白质溶液加入到层析柱中,弃去此时的流出液。
4) 在层析柱的出口处放置一个2ml的样品管,在层析柱中加入1ml PBS,收集流出的生物素标记蛋白质。
*经过层析,生物素标记蛋白质的最终浓度为标记时的1/2。
按照下列公式计算生物素标记蛋白质的最终浓度:
A (mol/l) = (X/MWprotein) × (1,000/Y) × 0.5
X:蛋白质的重量
MWprotein:蛋白质的分子量
Y:溶解蛋白质的NaHCO3缓冲液体积